Marcado UKCA
El marcado UKCA entró en vigor en Gran Bretaña en enero de 2021, cuando el Reino Unido abandonó la Unión Europea. El certificado UKCA puede ser necesario para determinadas clasificaciones de productos sanitarios y está disponible mediante los organismos aprobados designados por el Reino Unido, como BSI (0086). Existe un periodo de transición hasta el 30 de junio de 2023 para permitir que las certificaciones CE existentes sean sustituidas por el nuevo marcado UKCA. Sin embargo, la consulta para la nueva legislación del Reino Unido ha terminado; por lo tanto, la nueva legislación del Reino Unido debería publicarse a finales de este año.
A partir del 1 de enero de 2021, los productos sanitarios/IVD deben registrarse en la MHRA antes de su comercialización en el Reino Unido, independientemente de que lleven el marcado UKCA o el marcado CE. Los períodos de gracia para el registro de los productos en función de su clase de riesgo han finalizado. Por lo tanto, es obligatorio registrar todos los productos en la MHRA antes de comercializarlos.
Para Irlanda del Norte, el MDR y el IVDR de la UE se aplican a partir del 26 de mayo de 2021 y del 26 de mayo de 2022, respectivamente. Incluso después del 1 de julio de 2023, se seguirá exigiendo el marcado CE para los productos comercializados en Irlanda del Norte y los fabricantes deberán cumplir la normativa de la UE.
Queremos aclarar algunos otros aspectos sobre el marcado UKCA en esta comunicación. En primer lugar, le rogamos que consulte nuestro documento detallado de preguntas frecuentes online, que recoge muchas de las preguntas que pueda tener en torno al marcado UKCA.
- Requisitos de etiquetado e IFU para el marcado UKCA
Es fundamental asegurarse de que el etiquetado y las instrucciones de uso se han actualizado para hacer referencia al marcado UKCA, si es pertinente. Las principales consideraciones en este ámbito son:
- El etiquetado debe hacer referencia al marcado UKCA, incluyendo el número del organismo aprobado, por ejemplo, BSI (0086), si un organismo aprobado ha participado en el proceso de evaluación de la conformidad
- Los productos pueden tener tanto el marcado CE como el UKCA en el etiquetado antes del 1 de julio de 2023, y el doble marcado seguirá siendo aceptado en el mercado de Gran Bretaña después del 1 de julio de 2023.
- Persona responsable del Reino Unido
Debe designarse una persona responsable del Reino Unido (UKRP por sus siglas en inglés) si el fabricante tiene su sede fuera del Reino Unido. Este es un requisito obligatorio para todos los productos con marcado UKCA o CE para los fabricantes de fuera del Reino Unido. Consulte los requisitos de la MHRA para el UKRP.
- Declaración de conformidad (DoC por sus siglas en inglés) requerida para el marcado UKCA
En los casos en los que se ha aplicado el marcado UKCA (incluso cuando los productos han tenido un doble marcado), su DoC debe actualizarse para el marcado UKCA. El DoC debe hacer referencia a los requisitos legislativos del Reino Unido, incluidas las referencias; la legislación correcta es Medical Devices Regulations 2002 (SI618), modificada posteriormente por los Reglamentos de salida de la UE de 2019 (SI 791) y 2020 (SI 1478).
- Legislación horizontal del Reino Unido y normas designadas
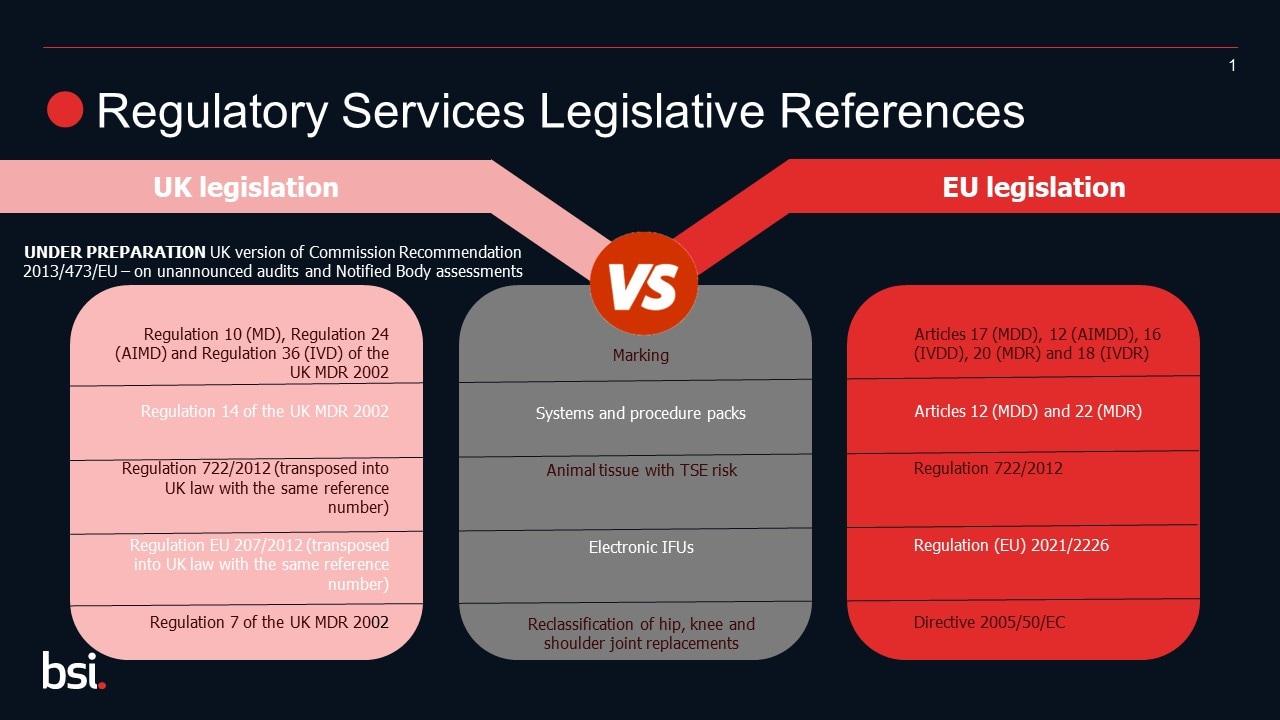
Las referencias de la legislación horizontal han cambiado como parte del UKCA; consulte el diagrama para evaluar sus requisitos.
Además, cuando el Reino Unido abandonó la UE, se rompió el vínculo con las normas armonizadas publicadas en el Diario Oficial de la UE. En consecuencia, el Reino Unido ha publicado su propia lista de normas que respaldan la normativa británica. Estas se han denominado "normas designadas".
Los fabricantes que utilicen normas para respaldar la conformidad de sus productos deben estar al tanto de la publicación de las listas de normas designadas en el Reino Unido y vigilar para obtener más información sobre el mantenimiento de estas listas.
¿Qué debo hacer ahora?
El marcado CE dejará de aceptarse para el mercado británico después de junio de 2023, y el marcado UKCA será obligatorio a partir de julio de 2023. Por lo tanto, asegúrese de que sus solicitudes contienen información actualizada para no causar retrasos indebidos en las revisiones.
BSI quiere preguntarle sobre sus planes actuales para permitirnos asignar la capacidad técnica necesaria. Por favor, ¿podría dedicar 10 minutos a completar nuestra encuesta para ayudarnos a planificar los recursos como Organismo Aprobado por la UKCA?
Háblenos de sus planes UKCA rellenando este breve cuestionario.
Por favor, rellénelo antes del viernes 1 de abril de 2022.
¿A quién puedo dirigirme para obtener más información?
El 27 de abril celebraremos un webinar para dar a conocer las últimas novedades.
Si tiene preguntas o dudas, por favor consulte la página web de BSI en primer lugar, donde mantenemos información actualizada sobre el certificado de la UKCA. Si lo necesita, puede obtener más información a través de su gestor del programa de BSI.
Atentamente,
Vishal Thakker
Head of UK Approved Body,
Servicios regulatorios (productos sanitarios)



