医薬品医療機器等法下におけるサーベイランス審査につきまして、BSI では下記のとおり審査または確認を実施させていただきます。
サーベイランス審査は製造販売業者等の品質管理監督システムごとの審査を概ね1年毎に実地調査にて実施させていただきます。
審査実施時期につきましては、基準月の -1ヶ月 / +1ヶ月の3ヶ月の間で調整いたします。
3ヶ月間以外での実施を希望される場合、基準月の変更をご希望される場合はご連絡ください。
BSIジャパンからサーベイランス審査の実施をご希望される場合
■ 申請時期 ■
- 基準月の3ヶ月前を目安に申請書類を郵送でご提出ください。
■ 申請書類 ■
- サーベイランス審査対象となる製造販売業者等の品質マニュアル及び組織図
- QMS適合性調査対象事業者の責任者等情報 (参考テンプレート ダウンロードページへ)
- ISO13485認証書コピー及び直近の審査報告書(該当する場合)
その他は実地審査の際に確認いたします。
■ 審査の流れ ■
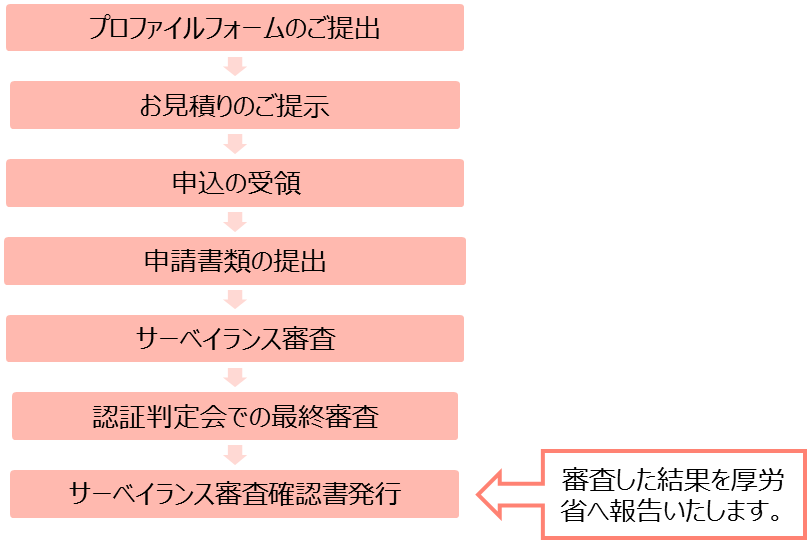
*製造販売業者がBSIジャパンからISO13485認証を取得されている場合は、ISO13485に合わせて弊社からご案内いたします。
他の登録認証機関によるサーベイランス審査をもってみなす場合
QMS適合性調査の実施をもってサーベイランス審査をみなす場合
■書類提出時期■
- 基準月の1ヶ月前を目安に書類をPDFでご提出ください。
- 1ヵ月前の提出が難しい場合は、予めご連絡いただけますと幸いです。
■ 提出書類 ■
- 他の登録認証機関による基準月より過去1年以内に実施された実地のサーベイランス審査報告書
- その他サーベイランス審査を確認したことが分かる書類
または
- 基準月より過去1年以内に発行された基準適合証のコピー
- 上記基準適合証のQMS調査結果総括報告書(BSI以外が発行した基準適合証を使用する場合)
- 有効なISO13485認証書のコピー(製造販売業者等の審査方法が書面でBSIジャパンからISO13485を取得していない場合のみ)
■ BSI確認の流れ ■
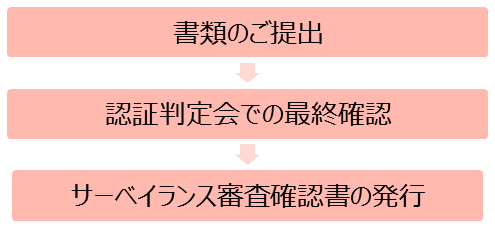
サーベイランス審査につきましては、下記通知等もご参照ください。


