Ist meine Software ein Medizinprodukt?
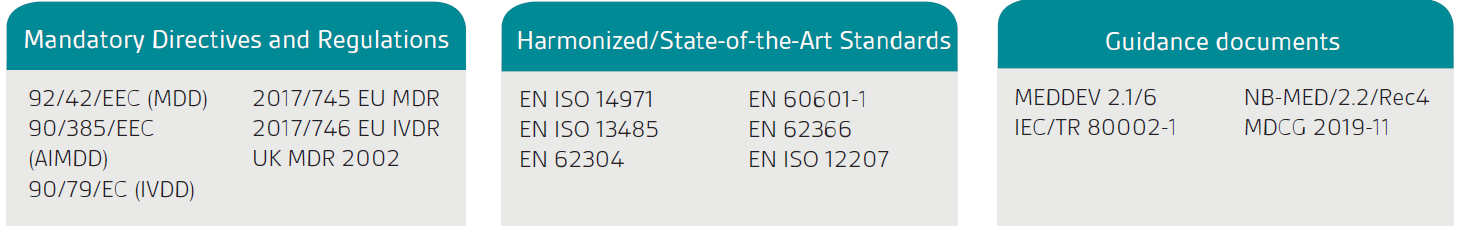
Zuerst müssen Sie prüfen, ob Ihr Produkt oder Ihre Dienstleistung rechtlich als Medizinprodukt (Software as a Medical Device, kurz SaMD) eingestuft wird. Das Produkt muss eine klare medizinische Zweckbestimmung im Sinne der Medizinprodukterichtlinien und -verordnung in der EU und/ oder der britischen Medizinprodukteverordnung (UK MDR) 2002 erfüllen.
Der Leitfaden der Europäischen Kommission, MEDDEV 2.1/6, gilt nur für Standalone Software.
Gemäß EU MDD/MDR und UK MDR wird Standalone Software (eigenständige Software), die eine medizinische Zweckbestimmung erfüllt, als ein aktives Medizinprodukt eingestuft. Die Klassifizierung richtet sich nach dem Risiko für den Patienten und die Anwender. Für eine vollständige Klassifizierung Ihrer Software, prüfen Sie bitte alle relevanten Klassifizierungsregeln.


 What regulators expect from medical device manufacturers of software with artificial intelligence (AI) and machine learning (ML)?
What regulators expect from medical device manufacturers of software with artificial intelligence (AI) and machine learning (ML)?