본 과정은 유럽 의료기기 규정(MDR)과 ISO 13485의 요구사항을 정확히 이해하고 실무에 적용할 수 있도록 구성되었습니다. MDR QMS 심사 준비와 부적합 대응, 사후관리 문서화 등 실무 역량 강화를 목표로 합니다. 유럽 인증 획득 및 유지에 필요한 최신 규정과 심사 대응 체계를 체계적으로 습득할 수 있습니다.
▒ 교육대상
• 의료기기 산업에서 이미 심사 경험이 있는 RA, QM, QA 담당자
• CE 인증 또는 QMS(MDR) 구축 프로젝트 참여자 및 인증 관련 실무 담당자
• 의료기기 제조사와 협력하는 주요 공급업체, OEM, 공식 대리인, 수입업자, 유통업자 등
심사 관련 조직의 직원
• ISO 13485:2016 및 MDR 요구사항에 익숙하고, 의료기기 QMS 실무 경험이 있는 자
(ISO 13485 선임심사원 또는 내부심사원 과정 수료자 권장)
▒세부사항
- 교육일정
3일(24시간), 비합숙
- 교육비용
100만원 (면세, 교재 제공)
▶ BSI 인증기업 : 교육비의 10% 할인
단, 할인쿠폰 발행 시에만 가능하오니,
BSI 교육팀(02-777-4123)으로 문의 부탁 드립니다.
- 교육장소
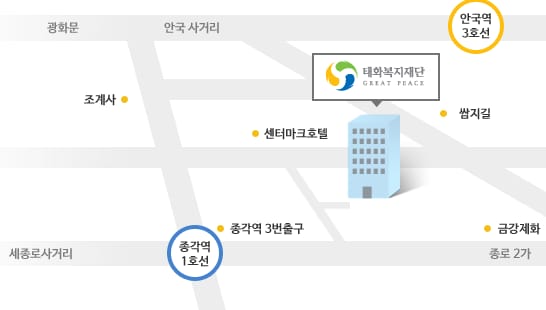
서울시 종로구 인사동 5길 29 태화빌딩 8층 BSI Training Center (03162)
(지하철 1호선 종각역 3번출구 도보3분)
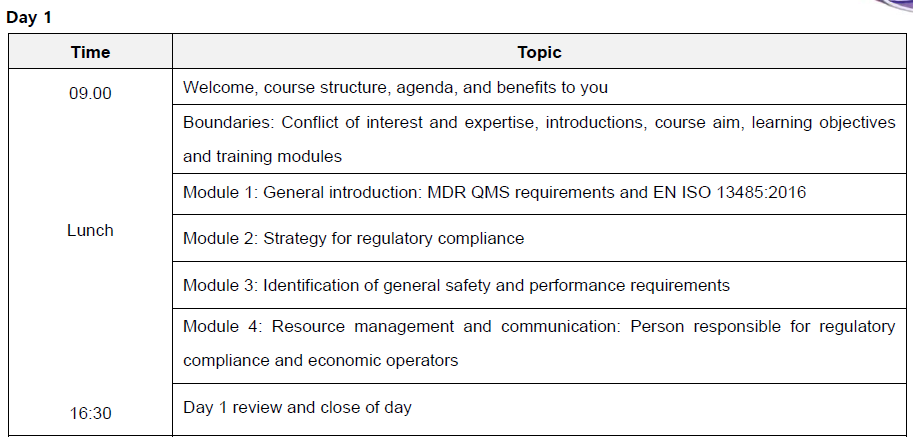
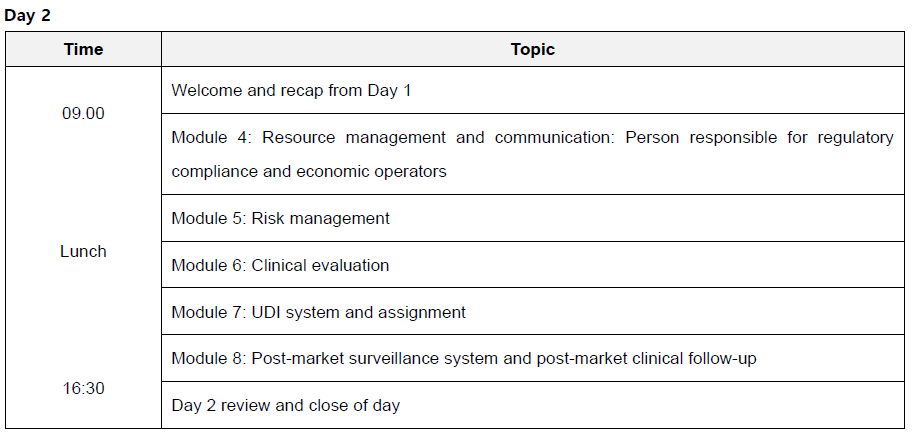
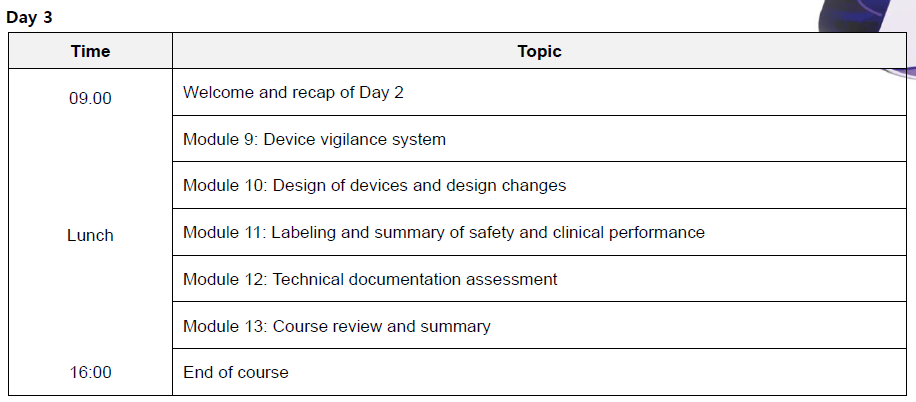
▒ 교육내용