BSI 的“医疗器械质量管理体系主任审核员培训(ISO 13485:2016)”课程旨在根据 ISO 19011“管理体系审核指导指南”以及 ISO 17021(如适用),讲授针对 ISO 13485 进行的有效质量管理体系审核的原则和实践。经验丰富的 BSI 讲师将指导学员熟悉整个审核流程 — 从启动审核直至进行审核后续跟踪。
让学员有信心地根据国际认可的最佳实践方法针对 ISO13485:2016 的要求对 QMS 进行有效审核。将您的专业知识与最新的发展相结合并且为您的质量体系的持续改进做出贡献,从而进一步增强患者安全。您将掌握根据 ISO 13485:2016 和 ISO 19011“管理体系审核指导方针”进行有效 QMS 审核的重要原则和实践方法。
使用分步式方法指导您熟悉从启动到后续跟踪的整个审核流程。五天的课程将使您掌握承担和领导成功的管理体系审核所需要的知识和技能。学习对 ISO 13485:2016 QMS 审核的目的进行说明以及满足第三方认证要求。您将掌握规划、执行、报告和跟踪 QMS 审核以确保符合性和增强整体组织绩效所需要的技能。
课程收益
所有参课学员需在课程最后一天进行考试。完成课程并通过考核的学员,将由BSI颁发CQI & IRCA注册课程培训资格证书,并可向 CQI & IRCA 申请成为国际注册主任审核员。
课程对象
• 管理代表
• 质量主管、经理
• 资讯顾问
• 法规部经理
• 执行该标准的相关部门组员
• 医疗器械工厂审核员(内审和外审)
• 对执行第一方、第二方或第三方审核感兴趣的医疗设备专业人员
课程目标
• 证明学员具备了承担和领导管理体系审核所需要的知识和基本技能
• 学员能够对质量管理体系的目的、质量管理体系标准的目的以及管理体系审核和第三方认证的目的进行说明
• 学员能够解释审核员在根据ISO 19011(和 ISO 17021(如试用)规划、执行、报告和跟踪质量管理体系审核方面所引起的作用
• 学员能够根据ISO 19011(和ISO 17021(如适用))规划、执行、报告和跟踪质量管理体系审核以证明是否符合ISO 13485的要求
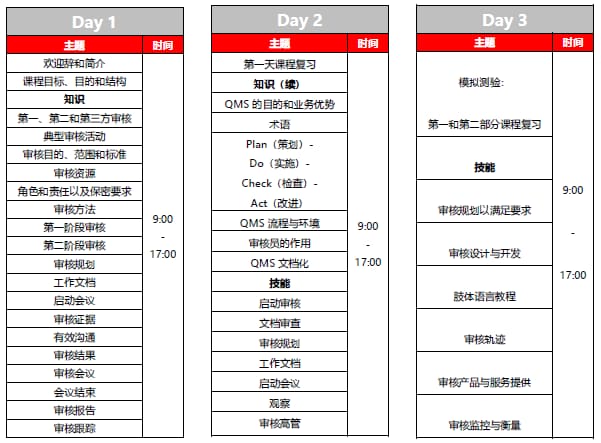
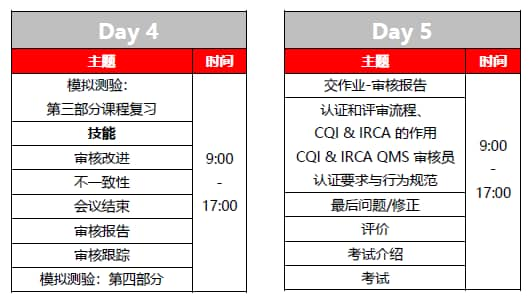
课程安排